Las imágenes médicas suelen ayudar a diagnosticar y tratar con éxito los tumores cancerosos. En particular, la resonancia magnética (RM) se utiliza ampliamente debido a su alta resolución, especialmente con medios de contraste.
Un nuevo estudio publicado en la revista Advanced Science informa sobre un nuevo agente de contraste nanométrico autoplegable que puede ayudar a visualizar tumores con mayor detalle a través de resonancia magnética.
¿Qué es el contraste?medios de comunicación?
Los medios de contraste son sustancias químicas que se inyectan en los tejidos u órganos humanos para mejorar la observación de imágenes. Estas preparaciones son más densas o menos densas que el tejido circundante, lo que crea un contraste que se utiliza para visualizar imágenes con algunos dispositivos. Por ejemplo, las preparaciones de yodo, sulfato de bario, etc., se utilizan comúnmente para la observación radiológica. Se inyectan en el vaso sanguíneo del paciente mediante una jeringa de contraste de alta presión.
A escala nanométrica, las moléculas persisten en la sangre durante períodos más largos y pueden penetrar en tumores sólidos sin inducir mecanismos de evasión inmunitaria específicos del tumor. Se han estudiado varios complejos moleculares basados en nanomoléculas como posibles transportadores de CA en tumores.
Estos agentes de contraste a nanoescala (NCA) deben distribuirse adecuadamente entre la sangre y el tejido de interés para minimizar el ruido de fondo y lograr la máxima relación señal-ruido (S/N). En altas concentraciones, el NCA persiste en el torrente sanguíneo durante períodos más prolongados, lo que aumenta el riesgo de fibrosis extensa debido a la liberación de iones de gadolinio del complejo.
Desafortunadamente, la mayoría de los NCA que se utilizan actualmente contienen conjuntos de varios tipos de moléculas. Por debajo de cierto umbral, estas micelas o agregados tienden a disociarse, y el resultado de este proceso no está claro.
Esto inspiró la investigación sobre macromoléculas nanométricas autoplegables sin umbrales críticos de disociación. Estas consisten en un núcleo graso y una capa externa soluble que también limita el movimiento de las unidades solubles a través de la superficie de contacto. Esto podría influir posteriormente en los parámetros de relajación molecular y otras funciones que pueden manipularse para mejorar la administración y especificidad de fármacos in vivo.
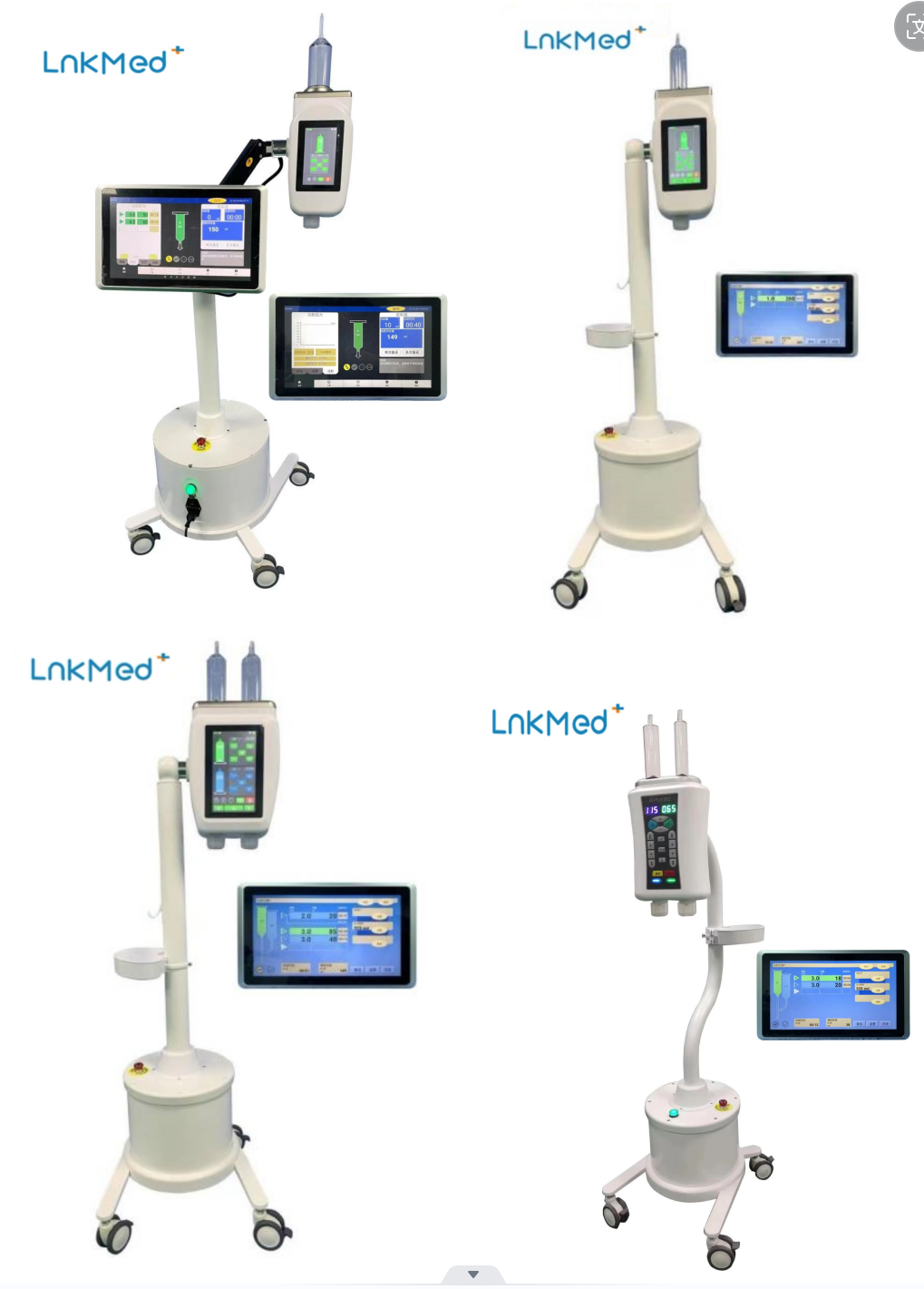
El medio de contraste generalmente se inyecta en el cuerpo del paciente a través de un inyector de contraste de alta presión.LnkMed, un fabricante profesional centrado en la investigación y el desarrollo de inyectores de agentes de contraste y consumibles de apoyo, ha vendido suCT, Resonancia magnética, yDSAInyectores nacionales e internacionales, reconocidos en el mercado de muchos países. Nuestra fábrica ofrece todo el soporte necesario.consumiblesActualmente popular en hospitales. Nuestra fábrica cuenta con estrictos procedimientos de control de calidad para la producción de productos, entregas rápidas y un servicio posventa integral y eficiente. Todos los empleados deLnkMedEsperamos participar más en la industria de la angiografía en el futuro, continuar creando productos de alta calidad para los clientes y brindar atención a los pacientes.
¿Qué muestra la investigación?
Se introduce un nuevo mecanismo en el NCA que mejora el estado de relajación longitudinal de los protones, lo que permite producir imágenes más nítidas con cargas mucho menores de complejos de gadolinio. Una carga menor reduce el riesgo de efectos adversos, ya que la dosis de CA es mínima.
Debido a la propiedad de autoplegamiento, el SMDC resultante presenta un núcleo denso y un entorno complejo y abarrotado. Esto aumenta la relajación, ya que el movimiento interno y segmentario alrededor de la interfaz SMDC-Gd puede verse restringido.
Este NCA puede acumularse en los tumores, lo que permite utilizar la terapia de captura de neutrones con Gd para tratarlos de forma más específica y eficaz. Hasta la fecha, esto no se ha logrado clínicamente debido a la falta de selectividad para administrar 157Gd a los tumores y mantenerlos en concentraciones adecuadas. La necesidad de inyectar dosis altas se asocia con efectos adversos y malos resultados, ya que la gran cantidad de gadolinio que rodea al tumor lo protege de la exposición a los neutrones.
La nanoescala facilita la acumulación selectiva de concentraciones terapéuticas y la distribución óptima de fármacos dentro de los tumores. Moléculas más pequeñas pueden salir de los capilares, lo que resulta en una mayor actividad antitumoral.
“Dado que el diámetro del SMDC es inferior a 10 nm, es probable que nuestros hallazgos se deban a la penetración profunda del SMDC en los tumores, lo que ayuda a escapar del efecto protector de los neutrones térmicos y garantiza una difusión eficiente de electrones y rayos gamma después de la exposición a los neutrones térmicos.“
¿Cuál es el impacto?
“Puede respaldar el desarrollo de SMDC optimizados para un mejor diagnóstico de tumores, incluso cuando se requieren múltiples inyecciones de resonancia magnética”.
“Nuestros hallazgos resaltan el potencial de perfeccionar el NCA a través del diseño molecular autoplegable y marcan un avance importante en el uso del NCA en el diagnóstico y tratamiento del cáncer”.
Hora de publicación: 08-dic-2023